细胞界大佬之CHO系列
第一篇
“前世今生”
哺乳动物CHO细胞系是目前表达制备生物制品最广泛的宿主,可以用来生产干扰素、白介素、EPO、单抗、诊断试剂和重组蛋白疫苗等药物。
如今,用CHO细胞表达的药品份额已经占到数千亿美元。作为细胞界的大佬,它的出现给整个全球生物制药产业注入了无穷的活力,产生了巨大的科研和经济价值。
正所谓没有谁能随随便便成功,CHO的发现与开发的背后也藏着一部血泪史,今天,让我们简单梳理一下CHO细胞的前世今生。
CHO细胞的前世今生
让我们把时间拨回到1919年,那时正值西班牙流感爆发,许多患者患上了肺炎。和现在医院的尖端诊断技术不同,当时为了判断肺炎的种类,医生需要培养患者肺部的细菌,而啮齿动物就是“试剂”。
可是在一百年前,小白鼠还没有普及,它们不仅少见还很昂贵。北京协和医学院E. T. Hsieh博士为了寻找小白鼠的替代品,在北京城里四处搜寻替代动物,意外发现了中国仓鼠(Cricetulus griseus)这一品种。这种仓鼠属于中国北部和蒙古地区的啮齿动物,数量很多,于是他就搞了一些来做实验,结果大获成功,从此中国仓鼠命运的齿轮开始转动……

1928年,还是协和医学院,有个叫Marshall Hertig的研究人员将150只中国仓鼠带到了哈佛医学院,希望将其建成一个品系,但可惜没能成功。
转眼到了1943年,现代遗传学先驱Guido Pontecorvo在低倍显微镜下观察中国仓鼠的染色体,发现只有14条(实际为2n=22),比起其它常用的实验鼠(小鼠的40条、大鼠的42条)要少,这使得中国仓鼠又多了一项送命奉献业务——用于染色体的研究。
渐渐地,越来越多的人知道了中国仓鼠对生物研究的价值,想要大量繁育,其中就有一名叫Victor Schwentker 的美国人,他在当时拥有美国东北部最大的实验动物饲养场,于是就委托正在中国研究疟疾的Dr.Robert Briggs Watson医生帮他进货。
1948年的冬天,Dr.Robert Briggs Watson冒着生命危险,带着20只由胡正祥教授赠予的中国仓鼠,穿过纷飞的战火历经千辛万苦运至美国旧金山,最后又转辗转到纽约成功交到Victor Schwentker手中。

大难不死,必有后福,经过Victor Schwentker两年的专门驯养,中国仓鼠终于被驯化成一种实验室动物品系,许多研究者慕名前来要货。这其中还有一个小插曲,哈佛大学的George Yerganian用更好的显微镜发现中国仓鼠有22条染色体,不是此前Pontecorvo报道的14条,即便如此小仓鼠们也拥有用于染色体研究的绝对优势。
时间加速到1957年,University of Colorado Medical Center的Dr.Theodore T. Puck和他的下属同事Fa-Ten Kao从波士顿癌症研究中心的Georege Yerganian博士的实验室获得了一个雌性中国仓鼠,然后开始用它的肺、肾脏、脾脏和卵巢的细胞进行体外培养。
实际上,和可以无限增殖的癌细胞不同,正常生物的细胞在分裂一定次数后就会死亡,在培养皿这样的异环境里就更不用提了。但是,这只中国仓鼠的卵巢细胞开了挂,它不但可以像癌细胞一样无限增殖,还完全适应了脱离肉体、活在硅基中的生活。
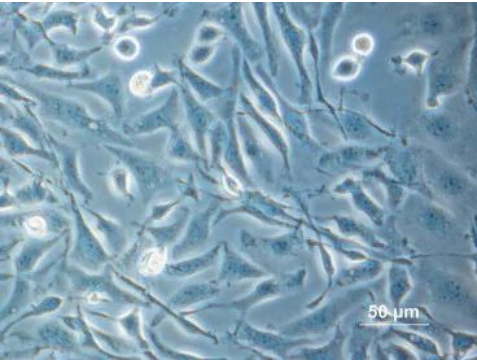
CHO 细胞系
这种可以无限增殖的能力叫做“永生化”,我们熟知的海拉细胞就在人体外实现了永生化。中国仓鼠的卵巢细胞是首个在培养皿内实现永生化的动物细胞,而且还是完全自发的。
就这样,Puck 成功用中国仓鼠卵巢的细胞并成功分离了CHO细胞系。很快,CHO 细胞系成了生物制药行业的标准细胞系,妥妥的团宠。就像大肠杆菌是微生物研究的标准生物一样,Puck 把 CHO 细胞叫做“哺乳动物中的大肠杆菌。”
1984年,Genentech公司首次实现重组中国仓鼠卵巢细胞表达组织型纤溶酶原激活剂(t-PA)并于1987年成功获批上市,标志着哺乳动物细胞表达系统生产蛋白药物的一个标志性事件。
随后,许多外源蛋白基因相继被转染到哺乳动物细胞,一些有价值的蛋白不断实现表达,包括凝血因子、促红细胞生成素(EPO)、免疫球蛋白、尿激酶、乙肝表面抗原(HBsAg)和单克隆抗体等,极大地促进了生物药工业的发展。
同时,随着CHO细胞在实验室的普及,科学家成功分离出的不同亚型的CHO细胞株,比如CHO-S, , CHO DXB11, CHO DG44,CHO-M以及近年来受到持续关注的GS基因敲除的CHO细胞(如Merck/Sigma Aldrich公司的CHOZN, Lonza的CHO GS Xceed, Horizon公司用rAAV技术敲除的CHO细胞)。
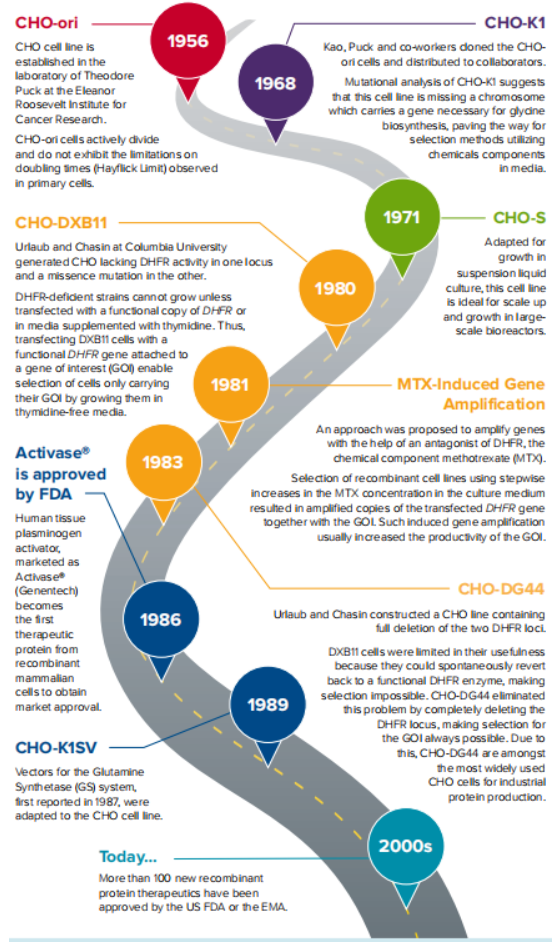
CHO细胞的绝对优势
CHO细胞在生物制药领域备受瞩目主要有以下几个原因:
一、CHO细胞遗传背景清晰,具有很高的安全性,以CHO作为宿主细胞表达生物蛋白质,容易被药物审核机构通过。
二、CHO细胞能用于表达各种复杂的重组蛋白。据统计:70%以上的动物细胞表达药物产品都是以CHO细胞为表达宿主。2011年6月批准的27种单克隆抗体中,其中13种就是通过CHO细胞表达的,占了约50%的比例。全世界批准正式应用于人类疾病治疗或疾病预防的基因工程产品约有三十多种,其中只有一种(乙肝疫苗)是由酵母菌生产的,其余所有产品都是由CHO细胞和大肠杆菌生产的,大肠杆菌不能形成有活性的二聚体(如白介素2),也不具有糖基化的功能(如EPO),而CHO却具有如上的功能,因此CHO成为表达复杂生物大分子的理想宿主。
三、CHO细胞属于成纤维细胞(fibroblast),是一种非分泌型细胞,它本身很少分泌CHO内源蛋白,因此对目标蛋白分离纯化工作十分有利。后来陆续又有后来陆续又有很多科学家用药物加压、极端条件筛选和诱导突变等方法筛选得到了一系列不同表型的CHO细胞株。
四、CHO细胞具有准确的转录后修饰功能,表达的糖基化药物蛋白在分子结构、理化特性和生物学功能方面类似于人员蛋白质翻译后修饰,如翻译后的糖基化修饰、唾液酸化修饰等。
五、CHO细胞具有外源重组基因的高效扩增和表达能力。目前CHO细胞已经开发出了多种商业化高效表达系统,如二氢叶酸还原酶筛选体系、谷氨酰胺合成酶筛选体系和遗传霉素筛选体系等。
六、CHO细胞既可贴壁生长也可以进行悬浮培养,且有较高的耐受剪切力和渗透压能力,外源蛋白表达水平较高,能够实现无血清培养基中快速及高密度生长,这为药物的质量控制和大规模生产带来极大的便利和实惠。
CHO残留检测
CHO、E.coli以及Vero细胞等作为生物制药产品的载体,其裂解释放出的DNA具有潜在的致瘤、致突变以及免疫原性等风险,因此世界卫生组织(WHO)、美国食品药品监督管理局(FDA)、欧洲药品管理局(EMA)及我国国家药品监督管理局(NMPA)等监管机构对生物制品成品的宿主DNA残留量都有严格的限制。
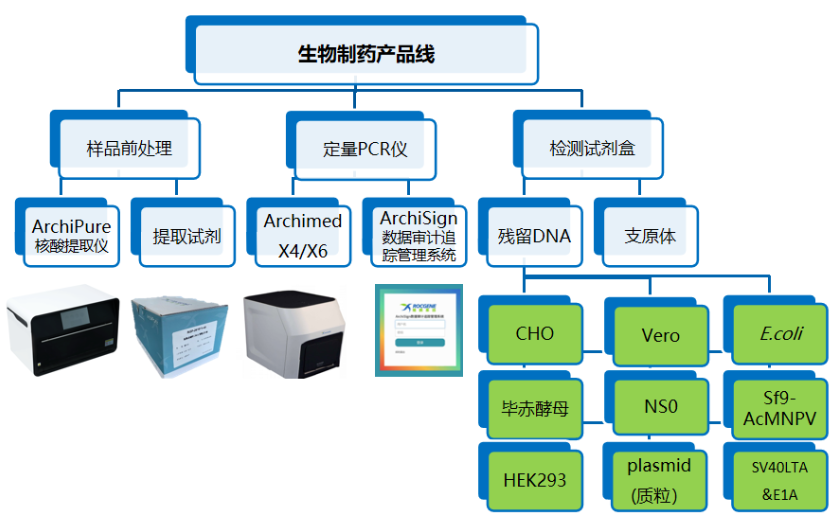
鲲鹏基因已开发的残留DNA检测系列产品,涵盖CHO、E.coli、Vero、NS0、Sf9&AcMNPV、HEK293、质粒、SV40&E1A 一系列宿主细胞残留DNA检测试剂盒,适用于鲲鹏基因的Archimed X 系列定量PCR仪以及7500、StepOne Plus和CFX96等众多机型。
同时配套开发了宿主细胞残留 DNA 提取试剂盒,及自动化核酸提取仪器。鲲鹏基因生物制药残留检测解决方案,包含样品前处理,定量PCR仪以及检测试剂盒整条产品线,助您轻松完成残留检测!
产品特点
1. 准确:试剂盒标准品溯源至国家标准品,检测值CV<5%;
2. 灵敏:可稳定检测fg级宿主DNA;
3. 快速:60分钟即可完成检测;
4. 防污染:dUTP+UNG酶体系,防止气溶胶污染;
5. 方便:全预混体系,无需体系配制,分装上样即检;
6. 性价比高:性能相当或更优,价格更实惠。
参考资料
Rawley JD.Theodore T. Puck (September 24, 1916–November 6, 2005). American Journal HumanGenetics 2006;78(3): 365–366.
Kim JY et al. CHO cells inbiotechnology for production of recombinant proteins: current state and furtherpotential. Applied Microbiology and Biotechnology 2012;93(3): 917–930.
Urlaub G; Chasin LA. Isolation of Chinesehamster cell mutants deficient in dihydrofolate reductase activity[J].Proceedings of the National Academy of Sciences U.S.A., 1980-07, 77 (7):4216-4220.
Landauer K, Woischnigg H, Hepp N et al (2011)Development of a chemically defined CHO medium by engineering based on a feed solution.BMC Proc 5(Suppl 8):P41
CHO MEDIA PLATFORM FACILITATES INTEGRATED CELLLINE DEVELOPMENT AND MEDIA OPTIMIZATION, IrvineScientic Poster in ESACT 2017

